Genoplivningen af stuetemperatur-natrium-ion-batterier
På grund af de rigelige natrium (Na)-reserver i jordskorpen og de lignende fysisk-kemiske egenskaber af natrium og lithium, har natriumbaseret elektrokemisk energilagring et betydeligt løfte for storskala energilagring og netudvikling. For eksempel har højtemperatur nul-emission batteriforskningsaktivitetsceller baseret på Na/NiCl2-systemer og højtemperatur Na-S-celler, som er vellykkede kommercielle tilfælde af stationære og mobile applikationer, allerede demonstreret potentialet i natriumbaserede genopladelige batterier. Men deres høje driftstemperatur på omkring 300 °C forårsager sikkerhedsproblemer og reducerer rundrejseeffektiviteten af natriumionbatterier (SIB'er). Rumtemperatur (RT) SIB'er betragtes derfor bredt som den mest lovende alternative teknologi til LIB'er.
I løbet af batteriernes historie i de sidste 200 år blev forskning i SIB'er glødende udført side om side med LIB-udvikling. Den elektrokemiske aktivitet af TiS2 for lithium og dets gennemførlighed til energilagring blev først fremført i 1970'erne. Efter denne opdagelse blev Na-ioners evne til at blive indsat i TiS+2 realiseret i begyndelsen af 1980'erne. Med opdagelsen af grafit som et billigt og moderat kapacitets anodemateriale til LIB'er og undladelsen af at interkalere natriumioner, skete en hurtig LIB-udvikling i 1990'erne, hvilket afløste væksten i natriumkemi. Så i 2000 foryngede tilgængeligheden til natriumlagring i hårdt kulstof (HC), som ville levere en energikapacitet svarende til Li i grafit, forskningsinteressen for SIB'er.
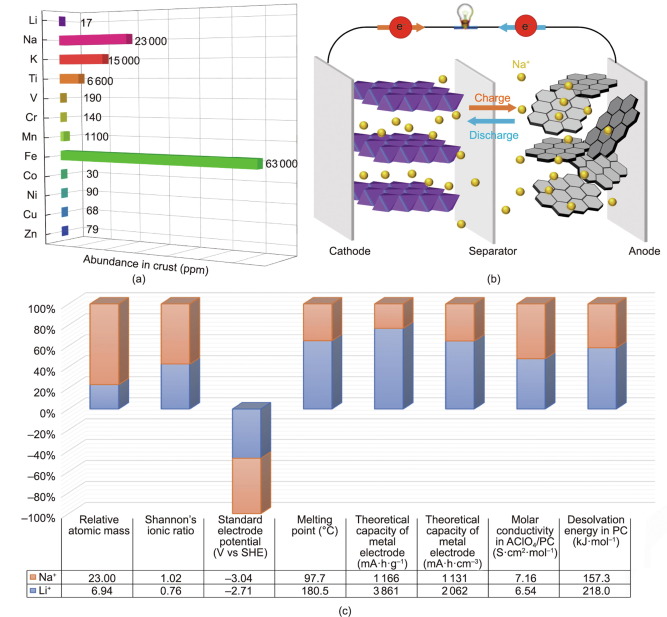
En sammenligning af natrium-ion-batteri og lithium-ion-batteri
Genoplivningen af SIB'er - kombineret med det stadigt stigende pres fra manglen på tilgængelighed af lithiumreserver og den tilsvarende eskalering i omkostninger - giver en komplementær strategi til LIB'er. SIB'er har fået stigende forskningsbevågenhed kombineret med fundamentale resultater inden for materialevidenskab i stræben efter at tilfredsstille den stigende udbredelse af vedvarende energiteknologier. Cellekomponenterne og de elektrokemiske reaktionsmekanismer for SIB'er er grundlæggende identiske med LIB'er, bortset fra ladningsbæreren, som er Na i den ene og Li i den anden. Hovedårsagen til den hurtige ekspansion i SIB-materialekemi tilskrives parallellerne i fysisk-kemiske egenskaber mellem de to alkalimetaller.
For det første svarer driftsprincipperne og cellekonstruktionen af SIB'er til dem for kommercielle LIB'er, omend med Na, der tjener som ladningsbærer. Fire hovedkomponenter findes i en typisk SIB: et katodemateriale (normalt en Na-holdig forbindelse); et anodemateriale (ikke nødvendigvis indeholdende Na); en elektrolyt (i flydende eller fast tilstand); og en separator. Under ladningsprocessen udvindes natriumioner fra katoderne, som typisk er lagdelte metaloxider og polyanioniske forbindelser, og indsættes derefter i anoderne, mens strømmen går via et eksternt kredsløb i den modsatte retning. Ved afladning forlader Na anoderne og vender tilbage til katoderne i en proces, der kaldes "gyngestolsprincippet". Disse ligheder har muliggjort den foreløbige forståelse af og hurtig vækst i SIB-teknologi.
Desuden bringer den større ionradius af Na sine egne fordele: øget fleksibilitet af elektrokemisk positivitet og nedsat desolvatiseringsenergi i polære opløsningsmidler. Det større mellemrum i den ioniske radius mellem Li og overgangsmetalionerne fører normalt til svigt af fleksibiliteten i materialedesign. I modsætning hertil muliggør et natriumbaseret system mere fleksible faste strukturer end et lithiumbaseret system og besidder enorm ionisk ledningsevne. Et typisk eksempel er β-Al2O3, hvor Na-interkalation har den perfekte størrelse og høj ledningsevne. Mere lagdelte overgangsmetaloxider med forskellige M+x+-stablingsmetoder kan nemt realiseres i et natriumbaseret system. Tilsvarende er den brede vifte af krystalstrukturer, der er kendt for natriumionlederfamilien (NaSICON) meget mere kompliceret end lithiumanalogerne. Endnu vigtigere er det, at en meget højere ionkonduktivitet kan tillades i NaSICON-forbindelser, som langt overstiger ionkonduktiviteten i lithiumioniske ledere (LiSICON)-forbindelser.
Sidst men ikke mindst har systematiske undersøgelser med forskellige aprotiske polære opløsningsmidler vist, at den større ionradius af Na forårsager en svagere desolvationsenergi. Den mindre Li har en højere overfladeladningstæthed omkring kernen end Na, når begge har samme valens. Li er derfor termodynamisk stabiliseret ved at dele flere elektroner med de polære opløsningsmiddelmolekyler. Det vil sige, at Li kan klassificeres som en type Lewis-syre. Som et resultat heraf er der behov for en relativt høj desolvatiseringsenergi for den stærkt polariserede Li, hvilket fører til en relativt stor overføringsmodstand, der induceres af transporten af Li fra den flydende tilstand (elektrolyt) til den faste tilstand (elektrode). Da desolvationsenergien er tæt forbundet med overførselskinetikken, der forekommer ved væske/faststof-grænsefladen, er den relativt lave desolvationsenergi en væsentlig fordel for at designe højeffekt SIB'er.